 |
Bleeding News
Febrero 2021
|
Compartir suscripción


|
|
 Variations and obstacles in the use of coagulation factor concentrates for major trauma bleeding across Europe: outcomes from a European expert meeting
Variations and obstacles in the use of coagulation factor concentrates for major trauma bleeding across Europe: outcomes from a European expert meeting
Vladimir Cerný, Marc Maegele, Vanessa Agostini, Dietmar Fries, Santiago R. Leal Noval, Gábor Nardai, Giuseppe Nardi, Anders Östlund, Herbert Schöchl
European Journal of Trauma and Emergency Surgery
(Abstract del artículo)
Autora del comentario:
Dra. Pilar Marcos. Medicina Intensiva. Hospital Germans Trias i Pujol, Badalona, Barcelona.
El traumatismo es una de las principales causas de muerte en el mundo (5,8 millones anuales). Los pacientes que presentan mayor riesgo de mortalidad son los que presentan un sangrado masivo. El 24-34% de ellos desarrollan coagulopatía inducida por el trauma (CIT) que agrava el sangrado y el pronóstico, por lo que su tratamiento mejora la supervivencia. Pero tanto la definición de CIT como su tratamiento no están claramente definidos en las diferentes guías europeas existentes. Este artículo recoge las recomendaciones de un grupo europeo multidisciplinar de expertos en trauma sobre la definición de CIT y su tratamiento, destacando el uso del concentrado de fibrinógeno humano (CFH) versus el de plasma fresco congelado (PFC).
Recordemos que para tratar la CIT, junto con los concentrados de hematíes (CH), disponemos de tranexámico (TXA), PFC y concentrados de factores de la coagulación (CFC) tales como el CFH, el concentrado de complejo protrombínico (CCP) y el crioprecipitado (hemoderivado rico en fibrinógeno y otros factores procoagulantes, poco disponible en España).
Tratamiento de la CIT según las guías europeas publicadas hasta abril 2018
¿En qué coinciden?
- En que el TXA debe administrarse lo antes posible.
- En que seguidamente se administrarán determinadas ratios de PFC:CH o CFH:CH (ambas opciones con evidencia 1C).
- En que se debe suplementar fibrinógeno con CFH o con crioprecipitado cuando los niveles de fibrinógeno estén bajos (evidencia 1C).
- En que el factor VII activado recombinante (rVIIa) no debe ser utilizado en primera línea.
¿En qué discrepan?
- En el nivel de fibrinógeno a partir del cual suplementar.
- En cuando utilizar el CCP en pacientes no tratados con fármacos antagonistas de la vitamina K.
¿Qué sugiere el grupo multidisciplinar de expertos en trauma?
1. Consideraciones en la definición de CIT:
✔ Tratar a los pacientes que están sangrando. No sólo a los que presentan parámetros de coagulación alterados en la analítica.
✔ Se considerará que un paciente traumático presenta CIT si está sangrando y en shock. Sugieren los siguientes grados de severidad:
1: Fibrinógeno < 1,5 g/L.
2: Fibrinógeno < 1,5 g/L e INR > 1,5.
3: Fibrinógeno < 1,5 g/L e INR > 1,5 con plaquetas < 100.000x10^9/L.
✔ Cuando se dispone de test viscoelásticos, el panel de expertos también está de acuerdo en la siguiente definición de CIT: EXTEM A5 (A5: máxima amplitud del test a los 5 minutos) ≤ 40 mm y/o FIBTEM A5 ≤ 9 mm.
✔ La ventaja de los test viscoelásticos son un diagnóstico de CIT más precoz. En los centros que no disponen de ellos sugieren utilizar un coagulómetro portátil.
2. ¿Cuándo activar el protocolo de transfusión masiva (PTM)?
✔ Por test viscoelásticos cuando FIBTEM A5 ≤ 9 mm.
✔ Si no disponemos de test viscoelástico y no tenemos el resultado de las pruebas de coagulación, el panel de expertos sugiere activar el PTM cuando:
- Sangrado severo y signos clínicos de hipoperfusión.
- Hipotensión (TAM < 65 mmHg o TAS < 100 mmHg).
- Exceso de base - 6 mmol/L.
- Hemoglobina ≤ 9 g/dL
✔ Tan pronto como sea posible se debe administrar TXA (dentro de las 3 primeras horas posteriores al trauma). Destacar los resultados favorables en los ensayos CRASH-2, CRASH-3.
3. ¿Por qué es tan importante suplementar el fibrinógeno?
Porque la depleción de fibrinógeno ocurre al inicio del trauma y persiste durante toda la hemorragia. Además, es el primer factor en alcanzar niveles críticos. Se ha descrito una reducción de la mortalidad (OR 0,22) con cada 1 g/L que incrementa el fibrinógeno al ingreso.
4. Consideraciones en el tratamiento de la CIT con fibrinógeno según el panel de expertos
✔ Se recomienda la administración de CFH, no la de PFC, tan pronto como sea posible después de la llegada del paciente al hospital, sin esperar a ningún test de laboratorio.
✔ Se recomienda suplementar el fibrinógeno cuando sus niveles sean < 1,5 g/L si persiste el sangrado o existe riesgo de sangrado mayor.
✔ En situación de emergencia se administrará una dosis estándar de 3-4 gramos de fibrinógeno. Si persiste el sangrado, dosis posteriores deben ajustarse por test viscoelástico o, si no se dispone de ellos, por peso (30-60 mg/Kg).
5. Consideraciones en el tratamiento de la CIT con CCP según el panel de expertos
✔ El déficit de trombina no es un problema en las fases iniciales del sangrado en el trauma, por lo que las recomendaciones en cuanto al uso de CCP son muy dispares entre guías.
✔ El panel de expertos sugiere tener controlada la hipofibrinogenemia y la posible hiperfibrinólisis del sangrado traumático antes de administrar CCP.
✔ Recomiendan únicamente la administración de CCP cuando el tiempo que tarda en iniciarse el coágulo esté alargado [CT (Clotting Time) del test viscoelástico].
6. Sugerencias para superar las barreras actuales para una administración eficaz de CFC
✔ Mejorar la educación mediante cursos online (ATLS, HEMACRIT) y mejorar el acceso a los test viscoelásticos.
✔ Ensayos clínicos que comparen la eficacia, coste-efectividad y riesgo trombótico del CFC vs PFC. Si bien estudios actuales sugieren que el riesgo trombótico asociado a CFC es bajo.
✔ Aconsejar que los centros dispongan de kits preparados con TXA, CFH, CCP además de CH al ingreso del paciente traumático (Kit de transfusión masiva).
7. Secuencia de tratamiento recomendada ante la CIT por el panel de expertos
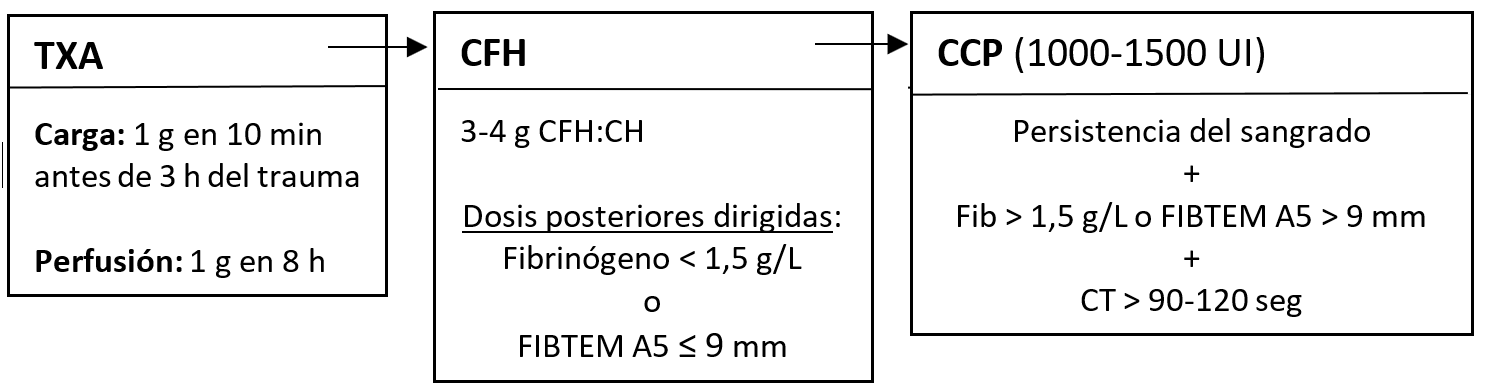
 Descargar PDF
Descargar PDF
 Institution of prothrombin complex concentrate protocols is associated with a reduction in plasma administration at a Tertiary Care Hospital
Institution of prothrombin complex concentrate protocols is associated with a reduction in plasma administration at a Tertiary Care Hospital
Louanne M Carabini, Ashley N Budd, Patricia Bochey, Shahriar Shayan, Glenn Ramsey, Robert J McCarthy
J Clin Anesth. 2021 Jan 21;70:110164. doi: 10.1016/j.jclinane.2021.110164.
(Abstract del artículo)
Autora del comentario:
Dra. Sonia María Veiras. Hospital Clínico Universitario de Santiago de Compostela. Jefe de Sección en el servicio de Anestesia y Reanimación. Provincia de A Coruña
En este estudio retrospectivo ubicado en un hospital terciario norteamericano, los autores analizan los cambios de consumo de plasma y de concentrado de complejo protrombínico (CCP) de 4 factores a lo largo de un periodo de seis años, durante los cuales el servicio de Farmacia del centro asistencial promovió cinco protocolos diferentes de aplicación del CCP de forma cada vez menos restrictiva, pasando de estar indicados en la reversión urgente de la warfarina en pacientes con hemorragia intracraneal a ampliarse su uso como parte del arsenal terapéutico de pacientes con sangrado masivo.
El consumo mensual de plasma y de CCP se estimó dividiendo las dosis totales administradas entre el número de ingresos mensuales, estableciendo previamente un modelo matemático de "estacionalidad" para ajustarse a la realidad de la distribución de los ingresos a lo largo de los diferentes periodos del año y para ajustarse también a una distribución normal.
49.245 unidades de plasma y 691 dosis de CCP fueron administradas en el periodo de estudio (76 meses). Se contabilizaron en total 289.319 ingresos hospitalarios excluyendo a la población obstétrica.
Los autores evidenciaron un descenso en el plasma mensual utilizado tras instaurarse protocolos de uso de CCP, siendo este descenso especialmente significativo en las áreas quirúrgicas y de cuidados intensivos, donde estos protocolos tuvieron la mayor relevancia clínica. El incremento en el empleo de CCP no fue comparable al descenso en el uso de plasma, lo que es interpretado por los autores como una mayor concienciación en el uso racional de los hemoderivados a raíz de la implementación de los diversos protocolos de uso de CCP.
Este trabajo pone de relevancia una realidad que nos toca a todos en nuestros centros de trabajo y que se puede resumir en varios puntos a modo de conclusiones:
1. El uso liberal e indiscriminado de plasma dispone de poca o nula evidencia científica y sin embargo es frecuente su empleo empírico en numerosas situaciones clínicas, en ocasiones incluso con fines profilácticos, lo que todavía es más difícil de aceptar desde el punto de vista científico.
2. Los CCP todavía no han adquirido ese papel de alternativa al plasma, quizá porque los criterios de uso y las indicaciones en ficha técnica son restringidos a la reversión de los anticoagulantes orales antagonistas de la vitamina K o en casos de deficiencia congénita de alguno de los factores de coagulación dependientes de la vitamina K cuando no se dispone de un producto purificado del factor específico.
3. El empleo de CCP en la reversión de los nuevos anticoagulantes orales (NACOs) o en las estrategias de control de sangrado masivo (ej. paciente politraumatizado) no se recogen como aprobados en ficha técnica.
4. La implementación y difusión de protocolos de estrategia de uso racional de los hemoderivados en los hospitales mejora la cultura del ahorro de sangre y la conciencia de su escasez y su no inocuidad en el empleo liberal.
Los CCP ofrecen varias ventajas evidentes sobre el plasma en los escenarios "oficialmente reconocidos" para su uso (la reversión de los anticoagulantes orales) que se pueden extrapolar a esas otras situaciones clínicas donde encontramos que los CCP tienen un espacio de utilidad franca:
- Rápida administración dado el pequeño volumen en que se diluye cada vial.
- Seguridad en pacientes con cardiopatía propensos a la entrada en fallo por sobrecarga de volumen (una unidad de plasma promedio contiene 250-300 ml mientras que cada vial de CCP se diluye en 20 ml)
- Para la administración de plasma debemos esperar al proceso de descongelado en el Banco de Sangre. Estas demoras pueden no ser aceptables en algunos escenarios clínicos.
- Los CCP están desleucocitados y difícilmente causarán reacciones a la infusión.
- El riesgo de desarrollo de TRALI (Transfusión Acute Lung Injury) es menor con el empleo de CCP al retirarse durante su manufactura los anticuerpos asociados con la lesión aguda pulmonar.
- El riesgo de transmisión viral se reduce con el uso de CCP al ser sometidos al menos a dos pasos distintos de inactivación viral durante su fabricación.
En resumen, se necesita una mayor apertura de las indicaciones aprobadas para la administración de CCP. Trabajamos más "cómodos" si estamos siguiendo directrices oficialmente reconocidas.
 Descargar PDF
Descargar PDF
 Whole Blood, Fixed Ratio, or Goal-Directed Blood Component Therapy for the Initial Resuscitation of Severely Hemorrhaging Trauma Patients: A Narrative Review
Whole Blood, Fixed Ratio, or Goal-Directed Blood Component Therapy for the Initial Resuscitation of Severely Hemorrhaging Trauma Patients: A Narrative Review
Mark Walsh, Ernest E. Moore, Hunter B. Moore, Scott Thomas, Hau C. Kwaan, Jacob Speybroeck, Mathew Marsee, Connor M. Bunch, John Stillson, Anthony V. Thomas, Annie Grisoli, John Aversa, Daniel Fulkerson, Stefani Vande Lune, Lucas Sjeklocha, Quincy K. Tran
J. Clin. Med. 2021, 10, 320.
(Abstract del artículo)
Autora del comentario:
Dra. Raquel Ferrandis Comes. FEA Anestesiología y Reanimación. Hospital Universitari i Politècnic La Fe, Valencia. Profesora asociada Facultad de Medicina de Valencia
Los autores plantean una visión global de un "eterno" dilema, contextualizándolo desde un punto de vista histórico y geográfico. Podríamos decir que llevamos mucho tiempo planteando la controversia entre el uso de sangre completa, una ratio fija de sangre:plasma:plaquetas o la sustitución guiada por objetivos, pero fue relativamente "ayer", en 2016 (en base al estudio PROPPR, publicado en 2015) cuando EEUU inició el uso de sangre completa en civiles, principalmente en centros con antecedentes militares. El estudio PROPPR, muy controvertido y criticado, mostró un benefició de la ratio 1:1:1 sobre 2:1:1 en la mortalidad por exsanguinación en las primeras 24 horas, pero no en otras causas de mortalidad.
Estos estudios han ido de la mano del desarrollo del concepto de coagulopatía inducida por el trauma, que se ha visto que no se evita con la transfusión de sangre completa o ratio 1:1:1 y que ha hecho decantar la balanza hacia el uso de terapias dirigidas por test viscoelásticos (VET) (primera publicación en 1997). La implantación de los VET ha sido mucho más amplia en Europa, liderados por el grupo alemán. En esta línea ha sido decisivo el estudio RETIC, que mostró la superioridad del fibrinógeno y el concentrado de factores sobre el plasma para el control de la coagulopatía por el trauma.
Los autores atribuyen esta diferencia geográfica a la mayor incidencia de heridas por arma blanca en EEUU frente a accidentes de tráfico en Europa, así como a la diferente organización del manejo prehospitalario. En este punto, dentro de la misma Europa, el índice de transfusión prehospitalario varia según el tiempo hasta la llegada al hospital. Además, en el manejo prehospitalario, los VET no están establecidos, ni en EEUU ni en Europa. En estos momentos, hay 3 ensayos clínicos en marcha para establecer el papel de la sangre completa en el manejo de la hemorragia masiva.
Con todo ello, los autores concluyen que los factores históricos, geográficos y logísticos juegan un papel primordial a la hora de decantar la balanza hacía un manejo basado en el VET (cada día más utilizado en Europa) o en sangre completa o ratio 1:1:1, aún predominante en muchos centros de EEUU.
 Descargar PDF
Descargar PDF
|
|
|
| |
|
|
|
| |
Comité Redactor: |
|
|
| |
Dra. Pilar Marcos
Medicina Intensiva.
Hospital Germans Trias i Pujol,
Badalona, Barcelona.
Dra. Sonia María Veiras
Hospital Clínico Universitario de Santiago de Compostela.
Jefe de Sección en el servicio de Anestesia y Reanimación
Provincia de A Coruña
Dra. Raquel Ferrandis Comes
FEA Anestesiología y Reanimación
Hospital Universitari i Politècnic La Fe, Valencia
Profesora asociada Facultad de Medicina de Valencia
|
Dr. Lluís Riera
Medical Scientific Liaison - Coagulación
CSL Behring Biotherapies for Life™
Dr. José Aznar
Director Médico en CSL Behring Biotherapies for Life™
|
| |
|
|
| |
|
|
|
|
|
|